Betegtájékoztató
1. MILYEN TÍPUSÚ GYÓGYSZER AZ AMINOMIX 1 NOVUM OLDATOS INFÚZIÓ ÉS MILYEN BETEGSÉGEK ESETÉN ALKALMAZHATÓ?
Az Aminomix 1 Novum oldatos infúzió intravénás alkalmazásra szolgáló gyógyszer. Beadása centrális vénán keresztül történik.
Az Aminomix 1 Novum a gyomor-bélrendszeren kívüli (parenterális) táplálásra szoruló felnőttek, illetve két évesnél idősebb gyermekek napi nitrogén- (aminosavak), energia- (glükóz), elektrolit- és folyadékszükségletének kielégítésére javallott (pl. amikor a szájon át történő táplálás nem lehetséges, nem elégséges, vagy ellenjavallt).
2. TUDNIVALÓK AZ AMINOMIX 1 NOVUM OLDATOS INFÚZIÓ ALKALMAZÁSA ELŐTT
Nem alkalmazható az Aminomix 1 Novum oldatos infúzió
- ,az aminosav-anyagcsere veleszületett zavarai
- súlyos májelégtelenség
- súlyos veseelégtelenség (művesekezelés a keringő vérmennyiség szűrésének hiányában)
- emelkedett szérumnátrium és -kálium-szint
- nem stabil anyagcsere (pl. súlyos lebontó anyagcsere (katabolizmus), nem stabil cukorbetegség (diabetesz mellitusz, tisztázatlan kómás állapot)
- súlyos kezelésre nem reagáló magas vércukorszint (hiperglikémia), csökkent glükóz-toleranciával nagy adag inzulin beadása ellenére is
- ismert túlérzékenység az infúzió bármely összetevőjével szemben
A nem szájon át történő táplálás általános ellenjavallatai:
- nem stabil, életveszélyes keringési állapotok (kollapszus és sokk)
- elégtelen sejt-oxigénellátás (hipoxia) vagy a vér vegyhatásának savas eltolódása anyagcsere zavar miatt (metabolikus acidózis)
- folyadék-túlterhelés (hiperhidráció) és/vagy heveny tüdővizenyő
- szíveredetű keringési zavar (pl.: dekompenzált szívelégtelenség/veleszületett szívelégtelenség)
Összetétele miatt az Aminomix 1 Novumot nem szabad újszülötteknek, csecsemőknek, és 2 év alatti gyermekeknek adni.
A kezelés megkezdése előtt a meglévő alacsony nátrium-koncentrációt korrigálni kell.
Az Aminomix 1 Novum fokozott elővigyázatossággal alkalmazható
A vércukorszint hirtelen változásainak megelőzése érdekében, ha az infúziót 24 óránál rövidebb időtartam alatt adják be, ajánlott az első órában fokozatosan növelni, az utolsó órában pedig fokozatosan csökkenteni az infúzió sebességét.
Az adagolást egyedileg kell meghatározni máj-, vese-, vagy mellékvese-elégtelenségben, illetve szív-, vagy tüdőelégtelenségben szenvedő betegek esetén.
A gyomor-bélrendszeren kívüli (parenterális) kezelés időtartama alatt a vércukorszintet, a szérum elektrolitokat, a sav-bázis egyensúlyt, a vízháztartás egyensúlyát és a vérképet rendszeresen ellenőrizni kell. Ha a vércukorszint jelentősen megnövekedne, az infúziót le kell állítani, és szükség esetén a vércukor csúcsértékeket kezelni kell.
A szokásosnál gyakoribb, rendszeres klinikai és laboratóriumi ellenőrzések különösen szükségesek az alábbiakban szenvedő betegekben:
- elégtelen aminosav-anyagcsere
- májelégtelenség (magas vér ammónia szinttel kapcsolatos, első ízben előforduló idegrendszeri rendellenességek, vagy meglévő neurológiai rendellenességek súlyosbodásának kockázata miatt)
- veseelégtelenség, különösen meglévő magas szérumkálium-szint esetén, ha fennállnak a vér vegyhatás savas eltolódásának anyagcsere zavara miatti (metabolikus acidózis), vagy súlyosbodásának kockázati tényezői, és elégtelen veseműködés eredményeként fellépő nitrogén tartalmú anyagok felszaporodása a vérben (azotémia)
- cukorbetegség (diabetesz mellitusz) (glükóz jelenléte a vérben (glikémia), cukortartalmú vizelet ürítése (glikozuria), ketontestek a vizeletben (ketonúria), inzulin adagolás)
- tejsavtúltengés és magas szérum ozmolaritás
Hosszan tartó alkalmazása során (több hét) a vérképet és az alvadási paramétereket figyelmesen ellenőrizni kell.
Különleges óvintézkedések gyermekekben történő alkalmazás esetén:
Az adagolást egyénileg kell meghatározni az életkornak, tápláltsági állapotnak, és az alapbetegségnek megfelelően, és szükség esetén a fehérjebevitelhez további szájon keresztüli (orális) vagy a gyomor-bélrendszeren kívüli (parenterális) készítményeket kell alkalmazni.
2 évesnél idősebb gyermekekben történő alkalmazás esetén nagyon lényeges, hogy olyan megfelelő méretű kiszerelést alkalmazzanak, amely a napi szükségletet egyetlen tartályban biztosítja.
Ezen felül lényeges a kezelés kiegészítése energiát, vitaminokat és nyomelemeket biztosító készítményekkel. Kiegészítőként gyermekgyógyászati készítményeket kell alkalmazni.
A kezelés ideje alatt alkalmazott egyéb gyógyszerek
Ez ideig nincsenek ismert kölcsönhatások.
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben szedett egyéb gyógyszereiről, beleértve a vény nélkül kapható készítményeket is.
Inkompatibilitások
Inkompatibilitás felléphet többvegyértékű kationok, pl. kálcium hozzáadásával, különösen heparinnal történő kombináció esetén. Szervetlen foszfátot nem szabad hozzáadni, a lehetséges kálcium- és magnézium-foszfát kicsapódás miatt.
Terhesség és szoptatás
Mielőtt bármilyen gyógyszert elkezdene szedni, beszélje meg kezelőorvosával vagy gyógyszerészével.
Ez ideig nincs tapasztalat az Aminomix 1 Novum alkalmazásával terhesség és szoptatás alatt. A termékenységre és a magzat fejlődésére kifejtett toxicitását állatkísérletekkel még nem vizsgálták, ezért használata terhesség és szoptatás alatt nem ajánlott. Mindemellett, ha az Aminomix 1 Novum használata a várható előnyök és kockázatok mérlegelésével feltétlenül szükségesnek látszik, az adása különös óvatosságot igényel.
A készítmény hatásai a gépjárművezetéshez és gépek kezeléséhez szükséges képességekre
Nem ismert.
3. HOGYAN KELL ALKALMAZNI AZ AMINOMIX 1 NOVUM OLDATOS INFÚZIÓT?
Adagolás és alkalmazás
Intravénás alkalmazásra, centrális vénán keresztül.
Az adagolást a beteg aminosav-, szénhidrát, elektrolit- és folyadékszükségletének megfelelően, valamint a klinikai állapotától (tápláltsági státusától és a rendellenesség által okozott lebontó anyagcsere súlyosságától) függően kell meghatározni.
A további energiaszükségletek kielégítésére megfelelő mennyiségű lipid emulzió adása javasolt.
Az infúzió adását az elérendő infúziós sebességnél alacsonyabb sebességgel kell kezdeni és 2-3 nap alatt kell a javallott sebességig növelni.
Felnőttek (ezen belül idősek) és 14 évesnél idősebb gyermekek:
Amennyiben másképp nem rendelik,
20 ml/ttkg/nap
= 1 g aminosav és 4 g glükóz/ttkg/nap
= 1400 ml/nap egy 70 kg súlyú beteg esetében.
A maximális infundálási sebesség:
1,25 ml/ttkg/óra
= 0,06 g aminosav és 0,25 g glükóz/ttkg/óra
A maximális napi adag:
30 ml/ttkg
= 1,5 g aminosav és 6 g glükóz/ttkg
= 2100 ml egy 70 kg súlyú beteg esetében
= 105 g aminosav és 420 g glükóz egy 70 kg súlyú beteg esetében.
A szénhidrátok alkalmazásának általános szempontjait és adagolási javallatait, valamint a folyadékbevitelre vonatkozó irányelveket figyelembe kell venni.
Normál anyagcsere-feltételek mellett a napi szénhidrátbevitelt 300-400 g-ra kell korlátozni. A korlátozásra a lehetséges oxidációs ráta kimerülése miatt van szükség. Az adag túllépésekor nemkívánatos reakciók, pl. zsíros májelfajulás jelentkeznek. Korlátozott anyagcsere-feltételek mellett, pl. posztagressziós anyagcsere esetén, oxigénhiányos állapotokban vagy szervelégtelenségben a napi adagot 200-300 g-ra (ami megfelel 3 g/ttkg-nak) kell csökkenteni; az adagolás egyéni adaptációja a beteg megfelelő ellenőrzését igényli.
A glükózra vonatkozó alábbi dóziskorlátozást szigorúan be kell tartani felnőttek esetében: 0,25 g/ ttkg/óra és legfeljebb 6,0 g/ttkg/nap.
A szénhidrátoldatok alkalmazása esetén, függetlenül azok koncentrációjától, szoros vércukorkontroll szükséges. Elsősorban nagyobb koncentrációjú oldatok alkalmazásakor a túladagolás elkerülésére a bevitel infúziós pumpán keresztül javasolt.
Gyermekek és 14 évesnél fiatalabb serdülők:
A gyermekekre vonatkozó adagolási javaslatok csak tájékoztató jellegű átlagértékek. Az adagolást egyénileg kell meghatározni az életkornak, fejlettségi foknak, és az alapbetegségnek megfelelően.
2 éves és idősebb, de 5 évesnél fiatalabb gyermekek napi adagja:
25 ml/ttkg ~ 1,25 g aminosav és 5 g glükóz/ttkg/nap
5 éves és idősebb, de 14 évesnél fiatalabb gyermekek napi adagja:
20 ml/ttkg ~ 1,0 g aminosav és 4 g glükóz/ttkg/nap
A maximális infundálási sebesség:
1,25 ml/ttkg/óra= 0,06 g aminosav és 0,25 g glükóz/ttkg/óra.
Az Aminomix 1 Novum biztonságát, tolerálhatóságát, és hatékonyságát gyermekekben és serdülőkben klinikai körülmények között még nem vizsgálták.
A kezelés időtartama:
Csak rövid- és középtávú gyomor-bélrendszeren kívüli (parenterális) táplálásra alkalmazható a beteg állapotától és a lebontó anyagcsere (katabolizmus) mértékétől függően, a javasolt adagolás betartása mellett.
A zsír, vitaminok és nyomelemek beviteléről azonban már a gyomor-bélrendszeren kívüli (parenterális) táplálás megkezdésekor gondoskodni kell.
Ezen kívül az oldat alkalmazható ugyanebben a terápiás javallatban, amikor a gyomor, -bélrendszeren keresztül történő táplálás nem elégséges, vagy nem lehetséges hosszabb időn keresztül, ha a zsír-, vitamin- és nyomelem-ellátás megfelelő.
Ha az előírtnál több Aminomix 1 Novum oldatos infúziót alkalmaztak
Nem megfelelő alkalmazás esetén (adagolás és sebesség) magas vércukorszint, folyadék-túlterhelés, a vér ozmotikus koncentrációjának emelkedése (hiperozmolaritás), a sav-, bázis- és elektrolitegyensúly-zavar jelei figyelhetőek meg.
Egyéb aminosav-tartalmú oldatokhoz hasonlóan a túl gyors infúziós sebesség kiválthat még hidegrázást, hányingert, hányást és növelheti a vesén keresztül történő aminosavvesztést.
Amennyiben ezek a tünetek fellépnek, az infúziót azonnal le kell állítani, vagy alacsonyabb infúziós sebességgel kell folytatni az adott esetnek megfelelően.
Magas vér káliumszint esetén ajánlatos 200-500 ml 10%-os glükózoldat infundálása inzulin hozzáadásával (1-3 E gyorshatású (nem módosított) inzulint számítva 3-5 g glükózra). Eredménytelenség esetén káliumkötő kationcserélő adása indokolt lehet. Vészhelyzetben a művesekezelés elkerülhetetlen.
Ha bármilyen további kérdése van a készítmény alkalmazásával kapcsolatban, kérdezze meg orvosát vagy gyógyszerészét.
4. LEHETSÉGES MELLÉKHATÁSOK
Megfelelő alkalmazás esetén az aminosavaknak és a glükóznak nincs ismert mellékhatása.
Más, nem a készítményhez, hanem általánosan a parenterális tápláláshoz kötött mellékhatások előfordulhatnak, különösen a parenterális táplálás kezdetekor.
Nem gyakori (1000 kezelt betegből több, mint 1, de 100 kezelt betegből kevesebb mint 1 esetén észlelhető):
Emésztőrendszeri betegségek: hányinger, hányás
Általános tünetek: fejfájás, hidegrázás, láz.
Ha bármely mellékhatás súlyossá válik, vagy ha a betegtájékoztatóban felsorolt mellékhatásokon kívül egyéb tünetet észlel, kérjük, értesítse orvosát vagy gyógyszerészét.
5. HOGYAN KELL AZ AMINOMIX 1 NOVUM OLDATOS INFÚZIÓT TÁROLNI?
Legfeljebb 25 °C-on, a külső védőborításban tárolandó.
A fénytől való védelem érdekében a zsákot tartsa a dobozában.
Eltarthatóság összekeverés után
A forrasztás átszakítása után, az összekevert kétrekeszes zsák kémiai és fizikai, alkalmazás közbeni stabilitása 24 órán keresztül biztosított. Mikrobiológiai szempontok miatt a készítményt azonnal fel kell használni a transzfer szett zsákhoz történő csatlakoztatása után.
Eltarthatóság kiegészítőkkel történő összekeverés után
Az átszakítható forrasztás felnyitása és a két oldat összekeverése után a kiegészítést a kiegészítő bemeneten keresztül lehet elvégezni.
Mikrobiológiai szempontok miatt a készítményt azonnal fel kell használni, miután az összekeverés megtörtént. Amennyiben azonnal nem kerül felhasználásra, a felhasználás előtti tárolási idővel és körülményekkel kapcsolatos felelősség a felhasználót terheli. Általában a keverék nem tárolható 24 óránál tovább 4-8 °C-on tartva.
A dobozon feltüntetett lejárati idő (Felhasználható) után nem alkalmazható az Aminomix 1 Novum oldatos infúzió. A lejárati idő a megadott hónap utolsó napjára vonatkozik.
Kizárólag akkor használható fel, ha mind az aminosav-, mind a szénhidrátoldat tiszta és a zsákok sértetlenek.
A zsák felnyitása után azonnal felhasználandó.
Minden felhasználatlan oldatot meg kell semmisíteni.
A gyógyszereket nem szabad a szennyvízzel vagy a háztartási hulladékkal együtt megsemmisíteni. Kérdezze meg gyógyszerészét, hogy szükségtelenné vált gyógyszereit miként semmisítse meg. Ezek az intézkedések elősegítik a környezet védelmét.
6. TOVÁBBI INFORMÁCIÓK
Mit tartalmaz az Aminomix 1 Novum oldatos infúzió
1000 ml oldatos infúzió tartalma:
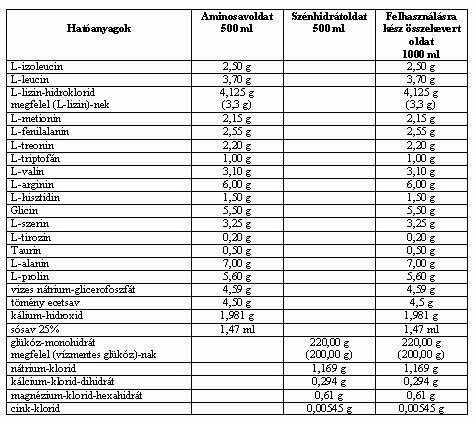
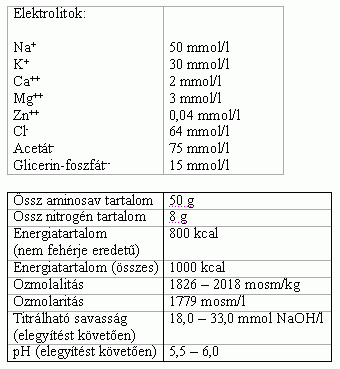
- Egyéb összetevők: higított sósav, nátrium-hidroxid, injekcióhoz való víz
Milyen a készítmény külleme és mit tartalmaz a csomagolás
Küllem:
Aminósavoldat: átlátszó, színtelen vagy halványsárga steril oldat.
Glükózoldat: átlátszó és csaknem színtelen, steril oldat.
Csomagolás:
6 x 1000 ml vagy 4 x 1500 ml vagy 4 x 2000 ml kétrekeszes zsák védőcsomagolással, kartondobozban.
A zsák felszakítható hegesztéssel 2 rekeszre van osztva. Az egyik rekesz kb. 500 ml vagy 750 ml vagy 1000 ml átlátszó, színtelen vagy halványsárga steril aminosavoldatot, a másik rekesz kb. 500 ml vagy 750 ml vagy 1000 ml átlátszó és csaknem színtelen, steril glükóz oldatot tartalmaz.
A zsák két kimeneti egységgel rendelkezik. A megtöltött infúziós zsák egy átlátszó külső védőzsákba van csomagolva, mely oxigén megkötőt tartalmaz.
Az LDPE/VLDPE/LLDPE/PP/PA zsák színtelen, átlátszó, műanyag.
A Biofine infúziós zsák polipropilént és termoplasztikus elasztomert tartalmazó színtelen, átlátszó, műanyag.
A védőcsomagolás többrétegű, poliolefin alapú filmből áll gátfunkcióval, amit poliészter/kerámia vagy etiléne-vinil-alkohol biztosít.