Modern medicina: betegség-betegség összefüggések nyomában - az interaktóma segítségével
A Semmelweis Egyetem OTDK tudományos előadásai között hangzott el Dr. Barabási Albert László összefoglalója. Részletesen szólt a Science magazinban egy hónappal megjelent, az elmúlt ötéves munkáját összefoglaló cikkről. Bizonyos betegséghez kapcsolódó fehérjék nem egyenletesen oszlanak szét a sejthálón belül, hanem koncentrálódnak a háló egy-egy specifikus részére. Ha ez bebizonyosodik, komoly hatással lesz a betegségek gyógyítására. Ehhez fel kell térképezni a fehérjehálókat, mert a térképek most még nagyon hiányosak. Véleménye szerint a hálózatkutatás a betegségek osztályzását is meg fogja változtatni amely a 19. század óta szinte változatlan...
(Az alábbiakban a Science-ben megjelent cikkükből idézünk néhány gondolatot.)
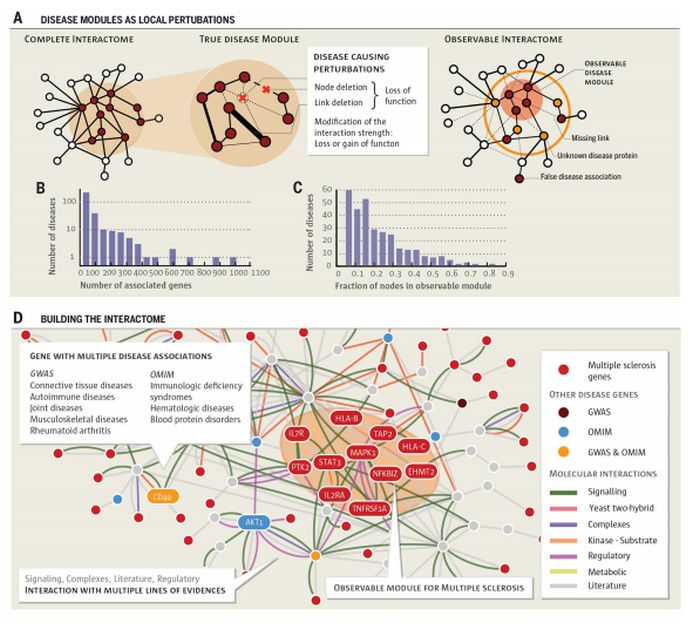
Bármely betegség általában nem egyetlen gén hibájának következménye, jellemzően multiplex molekuláris folyamatok konzekvenciájaként értelmezhető. E folyamatok kapcsolatait az ún. interaktóma kódolja, egy hálózat, amely adott sejt valamennyi fizikális „interakcióját” integrálja, a fehérje-fehérje, a fehérje-DNS és a metabolikus interakciókat egyaránt.
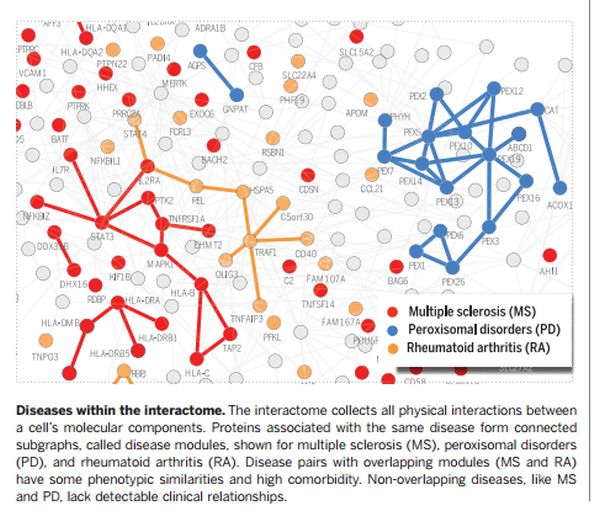
A betegségekkel kapcsolatba hozható fehérjék rendszere ún. betegségmodult alkot, ez lényegében egy gráf, amely tartalmazza a betegséggel kapcsolatba hozható valamennyi molekuláris szintű összetevőt. A betegségmodulok ilyen értelmű azonosítása lehet az első lépés a komplex betegségek molekuláris mechanizmusának megértéséhez. A tanulmány célkitűzése az egyes betegségmodulok lokalizációja, az egymástól akár jelentősen különböző betegségek közötti lehetséges kapcsolatok, átfedések elemzése volt.
Jelenleg e téren tudásunk még meglehetősen hiányos, annak ellenére, hogy az interaktóma-térkép, és a betegségekkel kapcsolatba hozható gének megismerése sokat fejlődött az elmúlt időszakban. Ez a hiányérzet vetette fel azt a kérdést, milyen mennyiségű adattömeg elegendő ahhoz, hogy a humán betegségek újfajta integratív megközelítését lehessen definiálni, részleteiben kidolgozni. Mindehhez megfelelő (bio)matematikai formulák képzése is szükséges, az interaktóma segítségével, a betegségek prediktivitásának mennyiségi analízise céljából.
A hálózatos modellek révén kimutatható volt, hogy csak azokat a betegség/modulokat lehet ezzel a megközelítéssel felfedni, ahol a betegséggel kapcsolatos gének száma meghalad egy kritikus küszöbértéket, éppen a rendszer inkomplett volta miatt. A kutatók szerint (jelenleg) 226 olyan betegség van, amelynél a fehérjék klaszterekbe rendeződése hasonló „környezetet” eredményez, vagyis statisztikailag is szignifikáns, azonosítható betegségmodulokat.
Itt a lényeg tehát: minél magasabb fokú az interaktómán belül a betegség-fehérjék „agglomerációja”, annál nagyobb a biológiai és funkcionális hasonlóság a megfelelő gének között is. Ezek az eredmények arra utalnak, hogy az interaktómán belüli betegségkörnyezet-modellek jól reprezentálják a valós betegségmodulokat. Amennyiben két (egymástól különböző) betegségmodul átfedésben van, az egyik betegséggel kapcsolatos helyi zavarok hatnak a másik betegség anyagcsere-útvonalaira is, azaz vannak közöttük hasonló klinikai és patobiológiai jellemzők.
Ez egyelőre hipotézis, ennek ellenőrzése céljából, betegségpárokat választottak a hálózaton belül, és direkt kapcsolatot figyeltek meg az egymástól eltérő, és relatíve távoleső betegségek patobiológiájában. Konkrétan: az átfedést mutató betegségmodulok esetén igen jelentps a molekuláris szintű hasonlóság, az összefüggésbe hozható gének expressziója, hasonlóak a tünetek – és magas a komorbiditás aránya is. Ugyanakkor a hálózatban, az egymással átfedést nem mutató betegségeknél nincsen patobiológiai kapcsolat. E modellel megjósolhatóvá válik olyan betegségek patobiológiai „rokonsága” is, amelyekben nem szerepelnek azonos gének.
Az interaktóma, mint modell a maga jelenlegi hiányosságaival együtt, alkalmas lehet a betegségek alapvető molekuláris mechanizmusainak leírására, kutatására. A hálózatos szemlélet nemcsak ebben, de a teljesgenom-szélességű (GWAS) vizsgálatokban, valamint a megfelelő gyógyszerek azonosításában is igen hasznos lehet a jövőben.
Az eredeti cikk néhány ábrája:
forrás: Semmelweis Hírek, Science
http://www.barabasilab.com/pubs/CCNR-ALB_Publications/201502-19_Science-Incomplete/201502-19_Science-Incomplete.pdf
Szponzorált tartalom



