Az EMA 2014 évi jelentése: az orvostudomány és az egészségügy fejlődése
Az Európai Gyógyszerügynökség rendes évi jelentése a szervezet kulcsfontosságú tevékenységeire koncentrált: a gyógyszerértékelésre, a kutatások szakmai támogatására az új és innovatív gyógyszereket illetően.
A tavalyi évben az EMA 102 új gyógyszer számára adott forgalomba hozatali engedélyt,ebből 82 humán és 22 a veteriner praxisban alkalmazott készítmény. Az árva gyógyszerként engedélyezett készítmények száma 63%-kal emelkedett, a humán gyógyszerekkel kapcsolatos szakmai tanácskérés is 16%-kal gyakoribbá vált az előző évhez képest.
A gyógyszerbiztonságossággal kapcsolatos tevékenység, a monitorozás minősége is javult a korábbiakhoz képest, nőtt a gyanított mellékhatás-bejelentések száma az EudraVigilance rendszeren keresztül. Ez konkrét számokban 6,5%-os növekedést jelent a humán, és 27%-ot a veteriner készítmények terén 2013-hoz viszonyítva.
Az EU-ban életbe lépett új farmakovigilanciával kapcsolatos rendelettel összefüggésben számos új aktivitás indult meg. Ilyen pl. a PSUR-tevékenység (periodic safety update reports) a nemzeti és centralizált törzskönyvezéseket követően, amelyek azonos hatóanyagra vonatkoznak.
Az éves jelentés kitér még néhány egyéb fontos szempontra: az EMA úgy döntött, hogy transzparenssé teszi a klinikai vizsgálatok adatait, amely igen jelentős előrelépés népegészségügyi és gyógyszerkutatási szempontból egyaránt.
A gyógyszerbevezetést illetően alternatív utakat kezdeményeznek (főként olyan terápiás területeken ahol nincsen gyógyszer, vagy igen csekély a terápiás választék), bevonják a betegeket, betegszervezeteket a gyógyszerekkel kapcsolatos haszon/kockázat értékelések folyamatába.
Néhány infografikát mutatunk az EMA tevékenységéről alább.
Kutatás-fejlesztés
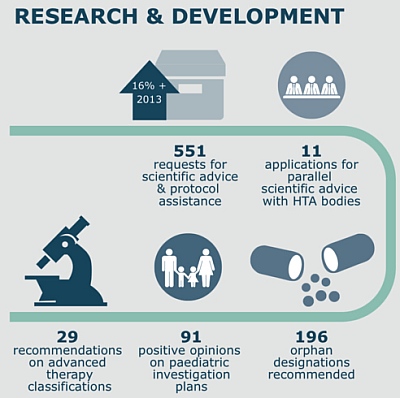
Törzskönyvezés
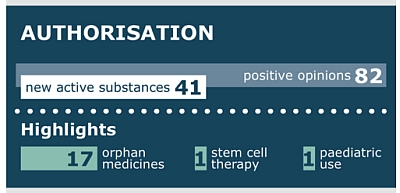
Mellékhatásbejelentés

Forrás, további információ
http://www.ema.europa.eu/ema/index.jsp?curl=pages/news_and_events/news/2015/04/news_detail_002320.jsp&mid=WC0b01ac058004d5c1



