Betegtájékoztató
1. Milyen típusú gyógyszer a Kevzara és milyen betegségek esetén alkalmazható?
Milyen típusú gyógyszer a Kevzara?
A Kevzara hatóanyaga a szarilumab. Ez egy fehérje, úgynevezett "monoklonális antitest".
Milyen betegségek esetén alkalmazható a Kevzara?
A Kevzara-t közepesen súlyos-súlyos aktivitású reumás ízületi gyulladásban (reumatoid artritiszben) szenvedő felnőttek kezelésére alkalmazzák, amennyiben a korábbi kezelés nem járt megfelelő eredménnyel, vagy azt nem tolerálták. A Kevzara önmagában vagy egy másik gyógyszerrel együtt is adható, amit metotrexátnak hívnak.
Segítségével:
- lassulhat az ízületeit érintő károsodás
- jobban elláthatja a mindennapi teendőit.
Hogyan hat a Kevzara?
- A Kevzara egy másik fehérjéhez, az úgynevezett "Interleukin-6" (IL-6)-hoz, kapcsolódik és gátolja a működését.
- Az IL-6 jelentős szerepet tölt be a reumatoid artritisz tünetei, például a fájdalom, duzzadt ízületek, reggeli ízületi merevség és fáradtság kialakulásában.
2. Tudnivalók a Kevzara alkalmazása előtt
Ne alkalmazza a Kevzara-t:
- ha allergiás a szarilumabra vagy a gyógyszer (6. pontban felsorolt) egyéb összetevőjére.
- ha aktív, súlyos fertőzése van.
Figyelmeztetések és óvintézkedések
Beszéljen kezelőorvosával, gyógyszerészével vagy a gondozását végző egészségügyi szakemberrel ha:
- bármilyen fertőzése van, vagy sokszor kap el fertőzést. A Kevzara csökkentheti szervezete fertőzésekkel szembeni ellenállóképességét - vagyis nagyobb valószínűséggel kaphat fertőzéseket vagy súlyosbíthatja az esetleg fennálló fertőzéseket.
- tuberkulózisban (tbc-ben) szenved, a tbc tünetei (tartós köhögés, fogyás, fásultság, hőemelkedés) állnak fel önnél, illetve ha közvetlenül érintkezett tbc-s beteggel. A Kevzara beadása előtt kezelőorvosa ellenőrizni fogja, nincs-e tuberkulózisa.
- volt már vírusos májgyulladása vagy egyéb májbetegsége. A Kevzara alkalmazása előtt kezelőorvosa vérvizsgálatot fog végezni a májfunkció értékelésére.
- volt már divertikulitisze (az alsó bélszakaszok rendellenessége) vagy fekélye a gyomrában vagy a beleiben, illetve ha nem múló tünetei, például láz és gyomor- (hasi) fájdalom alakulnak ki.
- valaha bármilyen rosszindulatú daganatos betegsége volt.
- a közelmúltban bármilyen védőoltást kapott vagy a jövőben kapni fog.
Ha a fentiek közül bármelyik igaz Önre (vagy ha nem biztos benne), szóljon kezelőorvosának, gyógyszerészének vagy a gondozását végző egészségügyi szakembernek a Kevzara alkalmazása előtt.
A Kevzara beadása előtt vérvizsgálatokat fognak végezni Önnél. A kezelés során is végeznek majd Önnél vizsgálatokat. Ennek az a célja, hogy ellenőrizzék, nem csökkent-e az alakos elemek száma a vérben, nincsenek-e májbetegségei illetve nem változott-e meg a koleszterinszintje.
Gyermekek és serdülők
A gyógyszer nem adható 18 évnél fiatalabb gyermekeknek és serdülőknek.
Egyéb gyógyszerek és a Kevzara
Feltétlenül tájékoztassa kezelőorvosát vagy gyógyszerészét a jelenleg vagy nemrégiben alkalmazott, valamint alkalmazni tervezett egyéb gyógyszereiről. Ennek oka, hogy a Kevzara befolyásolhatja néhány egyéb gyógyszer hatását. Néhány más gyógyszer pedig befolyásolhatja a Kevzara hatását.
Különösen fontos, hogy ne alkalmazza a Kevzara-t és szóljon kezelőorvosának vagy gyógyszerészének, amennyiben a következőket alkalmazza:
- az úgynevezett "Janus kináz (JAK)-inhibitorok" csoportjába tartozó gyógyszerek (olyan betegségben alkalmazzák, mint a reumatoid artritisz és rosszindulatú daganatok)
- a reumatoid artritisz kezelésére alkalmazott egyéb biológiai gyógyszerek
Ha a fentiek közül bármelyik igaz Önre (vagy ha nem biztos benne), szóljon kezelőorvosának vagy gyógyszerészének.
A Kevzara befolyásolhatja néhány egyéb gyógyszer hatását - ez azt jelentheti, hogy szükség lehet ezek adagjának megváltoztatására. Amennyiben a következő gyógyszerek bármelyikét alkalmazza, a Kevzara alkalmazása előtt szóljon kezelőorvosának vagy gyógyszerészének:
- sztatinok, a koleszterinszint csökkentésére szolgálnak
- szájon át alkalmazandó fogamzásgátlók
- teofillin, asztma kezelésére használják
- warfarin, vérrögképződés megelőzésére használják
Ha a fentiek bármelyike igaz Önre (vagy ha nem biztos benne), szóljon kezelőorvosának vagy gyógyszerészének.
Terhesség és szoptatás
Ha Ön terhes vagy szoptat, illetve ha fennáll Önnél a terhesség lehetősége vagy gyermeket szeretne, a gyógyszer alkalmazása előtt beszéljen kezelőorvosával.
- Terhesen ne alkalmazza a Kevzara-t - kivéve ha kezelőorvosa ezt kifejezetten javasolta.
- A Kevzara-nak a még meg nem született gyermekre gyakorolt hatásai nem ismertek.
- Kezelőorvosával együtt kell döntést hoznia arról, hogy szoptatás közben alkalmazhatja-e a Kevzara-t.
A készítmény hatásai a gépjárművezetéshez és a gépek kezeléséhez szükséges képességekre
A Kevzara alkalmazása várhatóan nem befolyásolja majd a gépjárművezetéshez és gépek kezeléséhez szükséges képességeket. Ha azonban a Kevzara alkalmazása után fáradt vagy rosszul érzi magát, ne vezessen gépjárművet és ne kezeljen gépeket.
3. Hogyan kell alkalmazni a Kevzarát?
A kezelést a reumatoid artritisz diagnózisában és kezelésében jártas orvosnak kell megkezdenie. A gyógyszert mindig a kezelőorvosa vagy gyógyszerésze által elmondottaknak megfelelően alkalmazza. Amennyiben nem biztos az adagolást illetően, kérdezze meg kezelőorvosát vagy gyógyszerészét.
Az ajánlott adag kéthetente egy 200 mg-os injekció.
- Vérvizsgálati eredményei alapján kezelőorvosa módosíthatja a gyógyszere adagját.
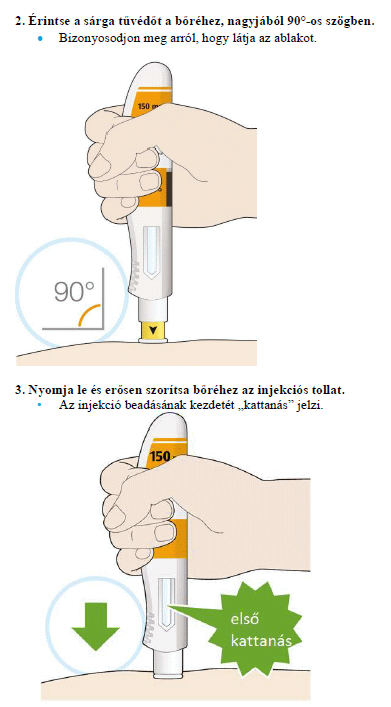
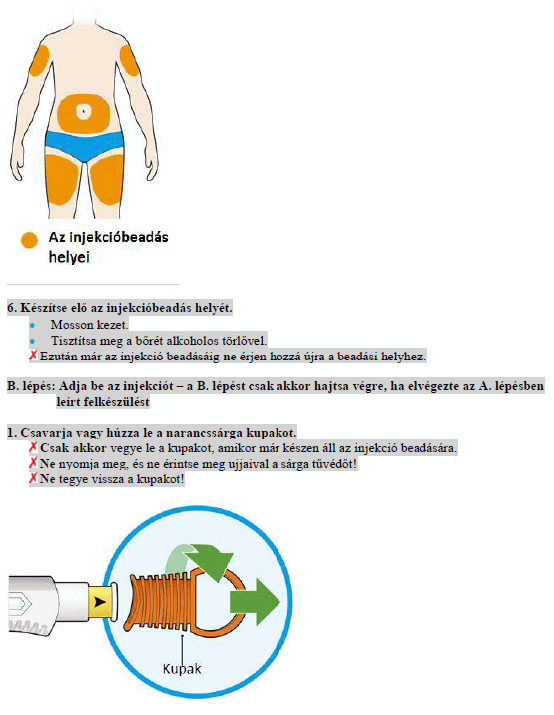
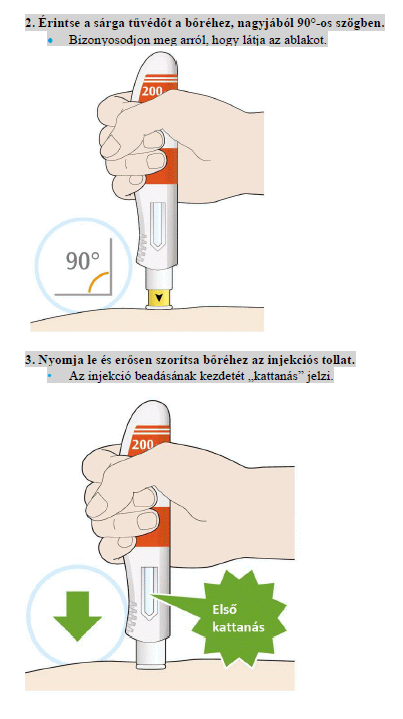
A Kevzara injekciót a bőr alá (úgynevezett szubkután injekcióként) kell beadni.
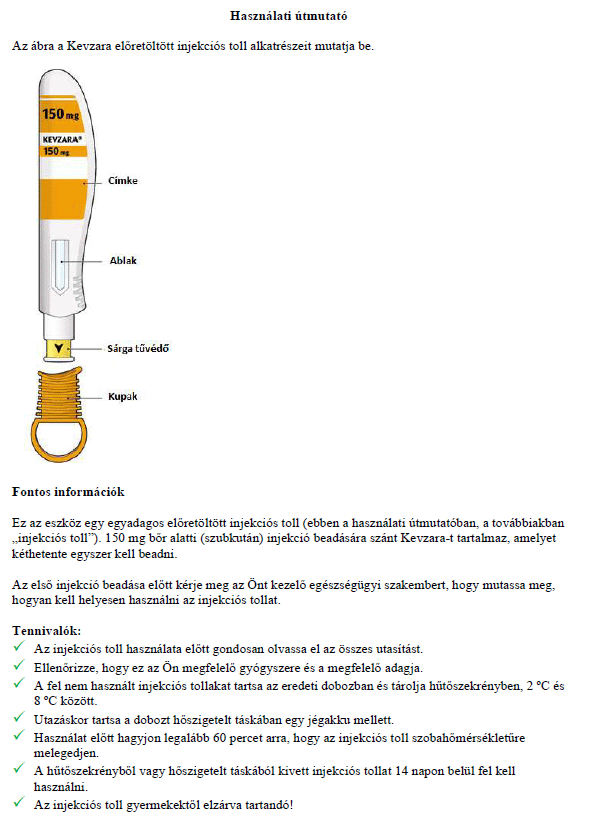
Az előretöltött injekciós toll alkalmazásának megtanulása
- Kezelőorvosa, gyógyszerésze vagy a gondozását végző egészségügyi szakember megmutatja, hogyan kell beadni a Kevzara-t. Ezeket az útmutatásokat követve saját maga vagy gondozója is beadhatja a Kevzara-t.
- Gondosan kövesse a dobozban található "Használati útmutató"-t.
- Pontosan a "Használati útmutató"-ban leírtak szerint használja az előretöltött injekciós tollat.
Ha az előírtnál több Kevzarát alkalmazott
Ha az előírtnál több Kevzara-t alkalmazott, szóljon kezelőorvosának, gyógyszerészének vagy a gondozását végző egészségügyi szakembernek.
Ha kihagyja a Kevzara egy adagját
Ha a kimaradt adag óta legfeljebb 3 nap telt el:
- a lehető leghamarabb adja be a kimaradt adagot.
- ezután a következő adagot a szokásos időben adja be.
Ha 4 vagy több nap telt el, a szokásos időpontban adja be az adagját. Ne adjon be kétszeres adagot a kihagyott adag pótlására. Ha nem biztos abban, mikor kell beadni a következő adagot, kérjen segítséget kezelőorvosától, gyógyszerészétől vagy a gondozását végző egészségügyi szakembertől.
Ha idő előtt abbahagyja a Kevzara alkalmazását
Ne hagyja abba a Kevzara alkalmazását anélkül, hogy beszélne kezelőorvosával.
Ha bármilyen további kérdése van a gyógyszer alkalmazásával kapcsolatban, kérdezze meg kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert.
4. Lehetséges mellékhatások
Mint minden gyógyszer, így ez a gyógyszer is okozhat mellékhatásokat, amelyek azonban nem mindenkinél jelentkeznek.
Súlyos mellékhatások
Haladéktalanul tájékoztassa kezelőorvosát, ha úgy gondolja, hogy valamilyen fertőzése van (ami 10 betegből legfeljebb 1 -et érinthet). Láz, verejtékezés vagy hidegrázás lehetnek a tünetek.
Egyéb mellékhatások
Mondja el kezelőorvosának, gyógyszerészének vagy a gondozását végző egészségügyi szakembernek, ha a következő mellékhatások bármelyikét észleli:
Nagyon gyakori (10 betegből több mint 1-et érinthet):
- Alacsony fehérvérsejtszám, vérvizsgálatokkal igazolt
Gyakori (10 betegből legfeljebb 1-et érinthet):
- a melléküregek és a torok fertőzései, orrdugulás vagy orrfolyás és torokfájás ("felső légúti fertőzés")
- húgyúti fertőzés
- szájban kialakuló herpesz ("ajakherpesz")
- alacsony vérlemezkeszám, amit vérvizsgálattal mutatnak ki
- magas koleszterin- és magas trigliceridszint, amit vérvizsgálattal mutatnak ki
- kóros májfunkciós vizsgálati eredmények
- az injekció beadásának helyén fellépő reakciók (beleértve a bőrpírt és a viszketést)
Nem gyakori (100 betegből legfeljebb 1-et érinthet)
- tüdőgyulladás
- a bőr mélyebb rétegének gyulladása
- a beleket érintő betegség, amely gyakran hasi fájdalommal, hányingerrel és hányással, lázzal és székrekedéssel, vagy ritkábban hasmenéssel jár (divertikulitisz)
Ritka (1000 betegből legfeljebb 1-et érinthet)
- gyomor- vagy bélperforáció (a gyomor- vagy bélfal átlyukadása)
Mellékhatások bejelentése
Ha Önnél bármilyen mellékhatás jelentkezik, tájékoztassa erről kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert. Ez a betegtájékoztatóban fel nem sorolt bármilyen lehetséges mellékhatásra is vonatkozik. A mellékhatásokat közvetlenül a hatóság részére is bejelentheti az alábbi elérhetőségek valamelyikén keresztül: Nemzeti Népegészségügyi és Gyógyszerészeti Központ, Postafiók 450, H-1372 Budapest, honlap: www.ogyei.gov.hu
elektronikus bejelentő form: https://mellekhatas.ogyei.gov.hu/
A mellékhatások bejelentésével Ön is hozzájárulhat ahhoz, hogy minél több információ álljon rendelkezésre a gyógyszer biztonságos alkalmazásával kapcsolatban.
5. Hogyan kell a Kevzarát tárolni?
A gyógyszer gyermekektől elzárva tartandó!
A címkén és a dobozon feltüntetett lejárati idő (EXP) után ne alkalmazza ezt a gyógyszert. A lejárati idő az adott hónap utolsó napjára vonatkozik.
Hűtőszekrényben (2 oC - 8 oC) tárolandó.
- Nem fagyasztható és nem melegíthető.
- A hűtőszekrényből kivett Kevzara legfeljebb 25 °C-on tárolható.
- Írja fel a hűtőszekrényből történő kivétel időpontját a dobozon megadott helyre.
- A hűtőszekrényből vagy hőszigetelt táskából kivett injekciós tollat 14 napon belül fel kell használni.
- A fénytől való védelem érdekében az injekciós tollat tartsa az eredeti dobozában.
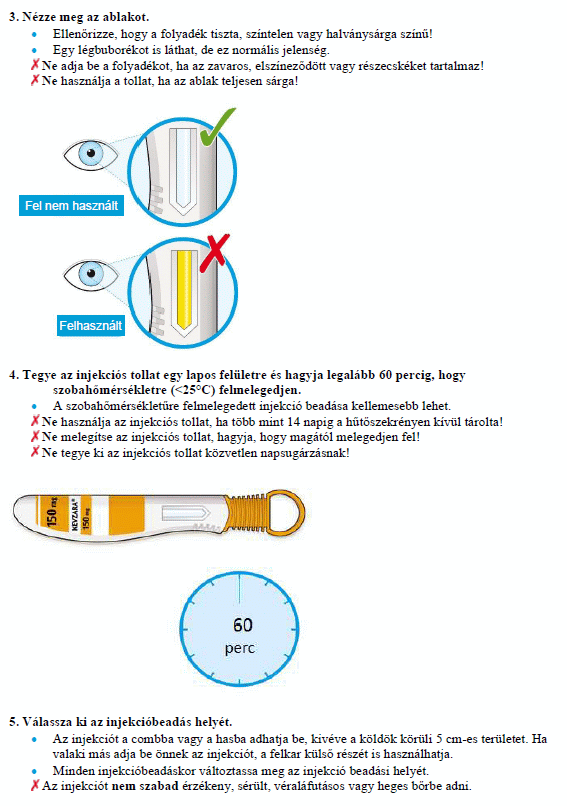
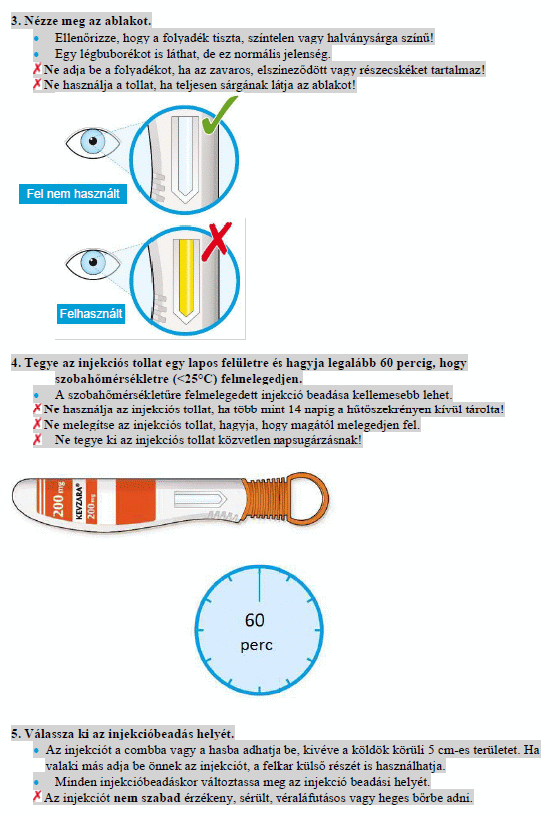
Ne alkalmazza ezt a gyógyszert, ha az injekciós tollban található oldat zavaros, elszíneződött vagy részecskéket tartalmaz, illetve ha az előretöltött injekciós toll bármelyik alkatrésze sérültnek tűnik.
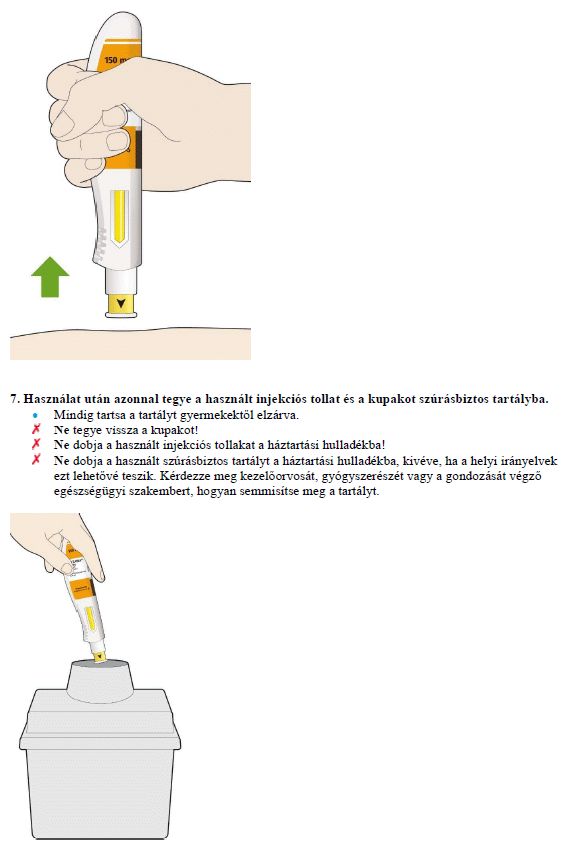
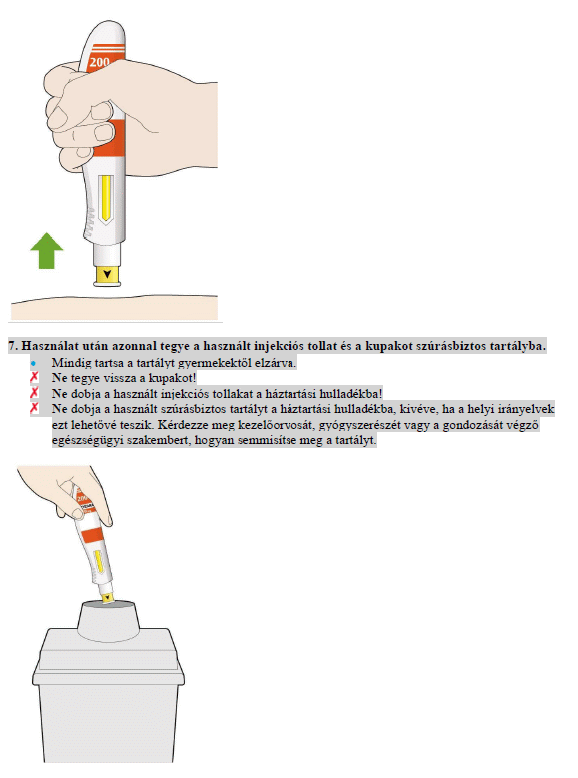
Használat után helyezze az injekciós tollat egy szúrásbiztos tartályba. Mindig tartsa a tartályt gyermekektől elzárva. Kérdezze meg kezelőorvosát, gyógyszerészét vagy a gondozását végző egészségügyi szakembert, hogyan semmisítse meg a tartályt.
Semmilyen gyógyszert ne dobjon a szennyvízbe vagy a háztartási hulladékba. Kérdezze meg gyógyszerészét, hogy mit tegyen a már nem használt gyógyszereivel. Ezek az intézkedések elősegítik a környezet védelmét.
6. A csomagolás tartalma és egyéb információk
Mit tartalmaz a Kevzara?
- A készítmény hatóanyaga a szarilumab.
- Egyéb összetevők: arginin, hisztidin, poliszorbát 20, szacharóz, valamint injekcióhoz való víz.
Milyen a Kevzara külleme és mit tartalmaz a csomagolás?
A Kevzara tiszta, színtelen-halványsárga oldatos injekció előretöltött injekciós tollban.
Mindegyik előretöltött injekciós toll 1,14 ml oldatot tartalmaz, amely egyetlen adag beadásához elegendő. A Kevzara 1 db vagy 2 db előretöltött injekciós tollat tartalmazó csomagolásban, vagy 3 db dobozt, dobozonként 2 db előretöltött injekciós tollat tartalmazó gyűjtőcsomagolásban kapható.
Nem feltétlenül mindegyik kiszerelés kerül kereskedelmi forgalomba.
A Kevzara 150 mg-os vagy 200 mg-os előretöltött injekciós tollban kapható.
Kevzara 150 mg oldatos injekció előretöltött injekciós tollban szarilumab
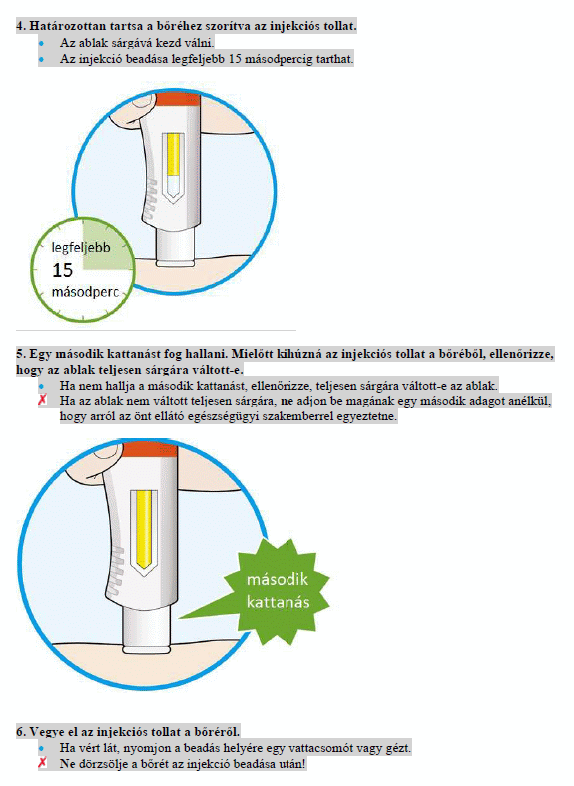
Használati útmutató